天气越来越冷,又到了“早上不想起,晚上不想睡”的季节!结束了一天的忙碌工作,躺在温暖的被窝里,拿起手机刷起来的那一刻,时间才真正的属于自己。等到缓过神来,“早睡计划”又又又泡汤了......
中国人的最新调查显示,我国居民整体睡眠质量欠佳,有59%的人存在失眠症状,另有28%的人群夜间睡眠时长甚至不足6小时。睡眠不足,比如睡眠时间短或失眠症状,已成为当代人的一大通病,折磨着中国超3亿人口。
睡眠不足可谓是健康的“慢性杀手”,会增加免疫病理学相关的多种疾病风险,包括心血管代谢、神经退行性、自身免疫病以及部分癌症。
先前开展的研究表明,当参与者的睡眠被限制或完全剥夺之后,能观察到核因子κB(NF-κB)信号通路被激活,表现为外周血液循环中白细胞介素-6(IL-6)水平增加、单核细胞IL-6表达增加,以及血液中C反应蛋白(CRP)水平增加。
简言之,炎症是睡眠不足导致上述慢性疾病的潜在机制之一;而反过来说,想要缓解睡眠不足带来的负面健康后果,一个可行的办法就是:从改善炎症入手。
提及抗炎,就不得不请出咱们的老朋友——阿司匹林(Aspirin)了!
近日,来自哈佛医学院的研究团队发现,低剂量的“百年神药”(约75-125mg/天)能够减轻睡眠不足带来的炎症反应,包括减少IL-6的表达,降低血清CRP水平,并抑制环氧合酶COX-1/COX-2双阳性细胞的数量等。没想到,阿司匹林还成了夜猫子的“救星”?

DOI:10.1016/j.bbi.2024.07.023
“百年神药”阿司匹林
睡眠不足时的炎症克星
一切还要从1897年说起,自德国化学家费利克斯·霍夫曼首次制备成阿司匹林以来,至今已有百余年的历史。
阿司匹林,又称乙酰水杨酸(ASA),作为首个被发现的非甾体类抗炎药,ASA可谓是当今世界上应用最广泛的解热、镇痛和抗炎药物。数据显示,全球每年消耗的阿司匹林约5万吨,合药片1200-5000亿片,甚至在临床上被称为“万能药”。
近年来,越来越多的研究发现了阿司匹林的新临床用途,比如治疗痛风、弥散性血管内凝血、代谢性肥胖、糖尿病及其周围神经病变、腹泻、脂肪肝等等。(详情可见:)
从机制上来看,低剂量ASA已被证明能够从多途径产生抗炎效果,包括抑制COX-1/COX-2酶的COX途径、以减少促炎细胞因子反应为核心的NF-κB途径,以及调节特异性促炎症消退介质(SPM)产生的炎症解决途径。
既然低剂量ASA能够从多途径实现抗炎,那么“万能药”是否也能改善睡眠不足带来的各种炎症反应呢?
连续5晚仅睡4小时
低剂量ASA会产生怎样影响?
这个问题引起了哈佛研究团队的好奇,他们设计了一项随机双盲交叉设计,纳入的46名参与者被随机分到三种方案中任意一个,三组分别为:睡眠不足+低剂量ASA组、睡眠不足+安慰剂组、正常睡眠+安慰剂组。
以睡眠不足+低剂量ASA组为例,也就是最主要的试验组。
正式试验开始之前,有14天的家庭检测阶段。在这2周的时间里,参与者得好好睡觉,每天都睡满8小时(23:00-7:00)。
在试验开始阶段,参与者有2个晚上可以好好睡一觉,他们被要求睡满23点至7点的8个小时,用于适应和基线测量。紧接着的5个睡眠不足的夜晚,他们只能在凌晨3点睡并在7点起来,连续5天只睡4个小时,听起来确实很痛苦。在此之后,有3天的恢复期,睡眠又回归正轨。
低剂量ASA给药控制在每天81mg,参与者会在每晚22点服用阿司匹林药片。而之所以选择夜晚服用ASA,也是经过研究员的深思熟虑的——有研究显示,睡前服用低剂量ASA比早上醒来之后服用更有益,能够有效减少晨间血小板聚集、降低24小时平均血压以及减少尿液中皮质醇和儿茶酚胺水平。
在整个实验阶段的第3天、第8天和第10天,参与者接受了血液采样、睡眠多导图记录和感觉测试。
另外两组就很好理解了,睡眠不足+安慰剂组就是将低剂量的ASA替换成安慰剂;正常睡眠+安慰剂组则每晚都好好睡觉,同时服用安慰剂。
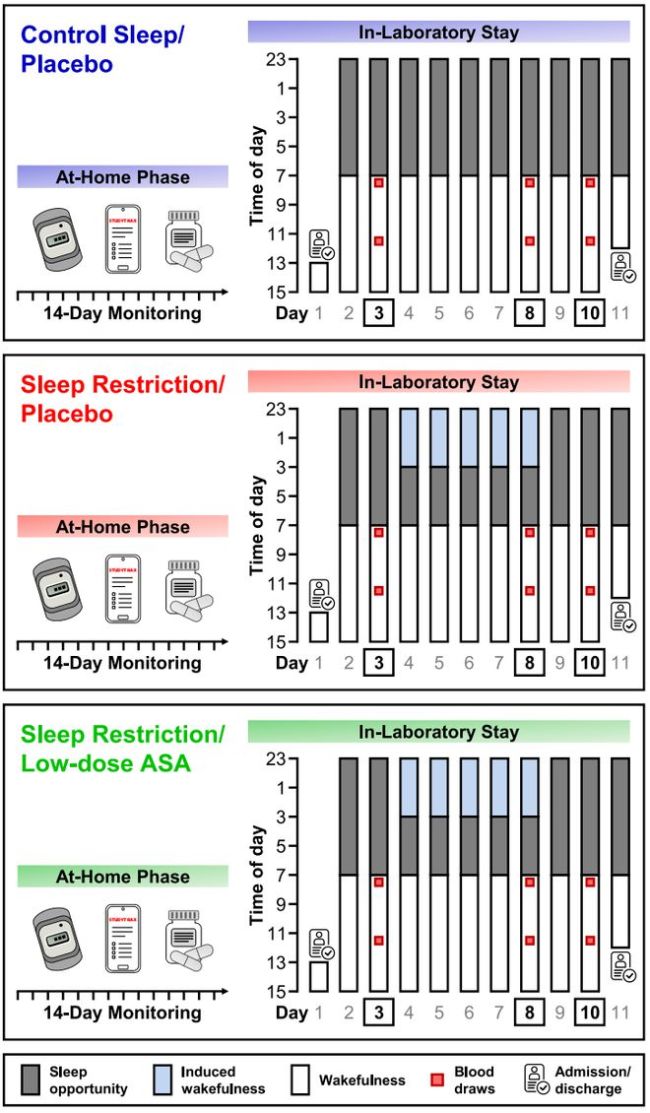
试验设计
双途径实现抗炎
效果接近于好好睡觉
事实上,服用阿司匹林并不会改变参与者的睡眠,无论是睡眠开始潜伏期(SOL,即从上床准备睡觉到真正入睡所经过的时间)和睡觉后清醒时间(WASO,即在入睡后到第二天早上醒来之间清醒的总时间),还是睡眠效率(SE,即实际睡眠时间与躺在床上准备睡觉的总时间之间的比例)都与安慰剂组没有差异。
仔细观察恢复期,还会发现低剂量ASA甚至改善了睡眠,包括睡着之后醒来时间的下降和睡眠效率的上升。整体来看,安全性还是有保障的。
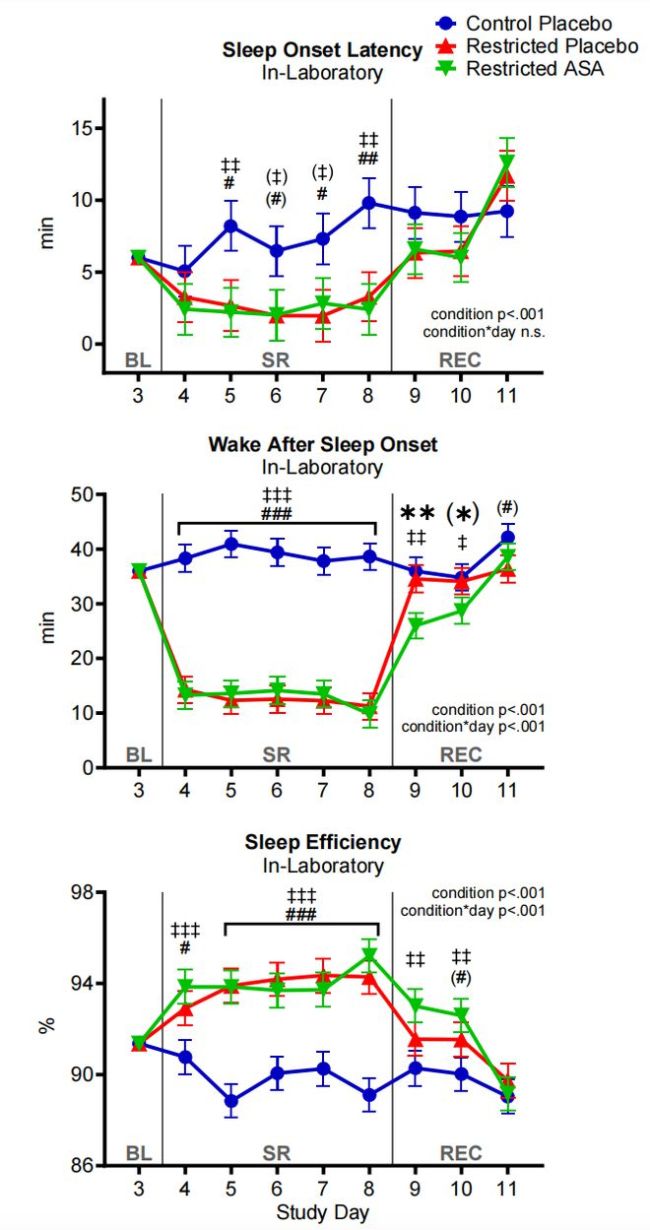
三组之间的睡眠情况差异
接下来就到了关键环节:“百年神药”阿司匹林会如何改善炎症呢?
从NF-κB途径切入,研究者观察到单核细胞中脂多糖刺激下的IL-6表达存在明显的条件 × 天数的交互作用效应。
具体来说,在连续五晚睡眠不足之后,IL-6飙升至最高值,但在恢复期又降至很低的水平。而如果熬夜的同时还服用了阿司匹林,效果就会大不一样——低剂量的ASA减少了睡眠不足引起的脂多糖(LPS)刺激单核细胞中IL-6表达的上升,从而使人体内IL-6水平的波动接近于正常睡眠组。
有意思的是,ASA并没有改变未刺激的单核细胞中IL-6表达。也就是说,服用阿司匹林不会影响正常基线炎症介质水平,而是针对性地抑制了睡眠不足带来的炎症反应,简直是“天选”的睡眠不足的炎症克星!
反观CRP水平,与先前报道的情况略有不同,在本项研究中,睡眠不足没有影响人体内的CRP水平。然而,服用小剂量阿司匹林的情况下,熬夜之后的CRP水平显著降低,甚至低于正常睡眠组。

ASA对NF-κB途径的影响
类似的,从COX途径来看,睡眠不足影响了人体内LPS刺激下的总COX-2水平,导致该数值明显升高,而服用ASA可逆转这一效果。
最大的差异出现在LPS刺激下COX-1/COX-2双阳性单核细胞的水平。在睡眠不足的情况下,LPS刺激的COX-1/COX-2共表达单核细胞显著增加;但补充了ASA之后,该数值明显下降且接近“正常睡眠”的情况。
令人惊讶的是,即使熬夜后恢复正常睡眠了,睡眠不足+安慰剂组的LPS刺激的COX-1/COX-2共表达单核细胞依然高于另两组,可见短短5天的熬夜“后劲很大”。
研究者表示,与单阳性细胞相比,双阳性或多功能免疫细胞往往更能说明问题,更具反应性和功能性。因此,COX-1/COX-2双阳性单核细胞水平的降低,很好地反映出小剂量“百年神药”对睡眠不足的抗炎作用。
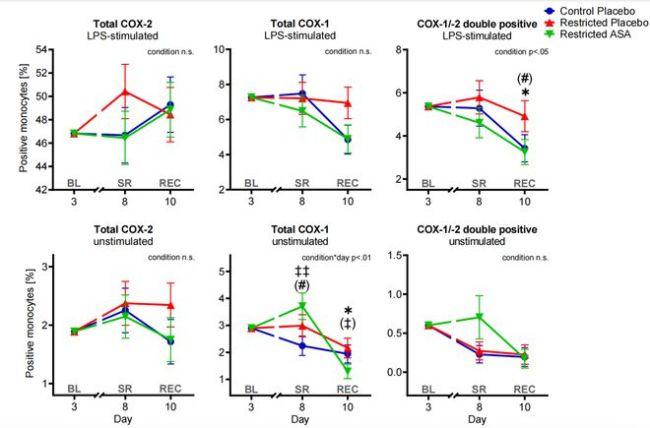
ASA对COX途径的影响
综上所述,睡眠不足会从NF-κB(负责促炎细胞因子和CRP的表达)和COX(掌控促前列腺素的形成)两大途径导致炎症的发生,但小剂量ASA能够减少促炎通路的激活,表现为降低了LPS刺激的单核细胞中IL-6表达和血清CRP水平,同时减少LPS刺激的单核细胞中COX-1/COX-2双阳性细胞的数量,从而缓解熬夜带来的炎症损伤。
因此,在你不得不熬夜的情况下,阿司匹林称得上是“健康卫士”,具有减少炎症和支持恢复性睡眠的潜力。但也要记住,阿司匹林并不是万能的,保证充足的睡眠才是王道,千万不要“本末倒置”了。





